*仅供医学专业人士阅读参考安徽润格
引言
补体C5抑制剂作为靶向补体系统的创新疗法,在自身免疫性神经疾病领域不断突破。在2025年6月21日~24日于芬兰 赫尔辛基召开的欧洲神经病学学会(EAN)年会上,多项研究聚焦于重症肌无力(MG)、视神经脊髓炎谱系疾病(NMOSD)等神经免疫疾病,从改善症状、降低复发风险到提升患者生活质量,展现出创新生物制剂的临床潜力。本文结合EAN2025年会上最新公布的14项研究数据,探讨MG疾病特征及补体抑制剂在神经免疫疾病领域的前沿进展,剖析其为患者带来的治疗变革与未来方向。
聚焦MG病理机制及临床特征,探索管理优化路径
研究亮点导读:
MG自身抗体聚类分析:首次基于5种抗体将MG分为两类自身抗体簇,其中簇2(RyR+/titin+/AChR+)患者病情更重、合并症更多。在真实世界中,明确抗体谱可指导MG分层治疗,高危患者需强化管理,有助于推动MGFA分型与抗体特征结合[1];
BEYOND研究:>60%经治gMG患者仍饱受症状波动困扰,80%患者认为更好控制可显著提高生活质量。该研究凸显现有治疗未满足需求,强调治疗上需以患者为中心,以功能恢复为目标,全面优化综合干预策略[2];
针对中国gMG急性加重患者的大样本真实世界研究:纳入476例gMG患者,全面分析急性加重期治疗模式、住院负担及临床结局。研究结果将有助于明确中国gMG急性加重的经济负担,推动医保覆盖优化,同时助力风险分层,指导急性加重标准化管理流程[3]。
MG临床特征与疾病负担
MG的自身抗体:聚类分析及临床相关性
该研究旨在探讨MG患者中自身抗体及其与临床特征的相关性,共回顾了664名MG患者的医疗记录,对检测出的5种自身抗体(AChR、MuSK、titin、RyR和LRP4)进行聚类分析,并比较了各聚类之间的不同临床表现,此外还进行了单独的关联分析,评估个体自身抗体与临床表现及不同MGFA亚型之间的关系[1]。
该研究发现了MG患者中存在两种独立的自身抗体簇,其临床表现存在显著差异:簇1中的485例患者以RyR抗体-、titin抗体-和AChR抗体-为主,簇2中的179例患者则以RyR抗体+、titin抗体+和AChR抗体+为主。簇2患者年龄更大,定量重症肌无力评分(QMG)更高,且高血压、糖尿病、心脑血管疾病及眼部病变等并发症发生风险显著增加。
个体抗体分析显示,男性患者更易出现AChR抗体阳性和titin抗体阳性,高龄则与AChR抗体、RyR抗体及titin抗体阳性相关。
MGFA分型比较发现,AChR抗体、MuSK抗体、titin抗体、并发症、胸腺瘤及高血压在不同亚型间存在显著差异。随着MG严重程度从I型进展至V型,AChR抗体、RyR抗体和titin抗体阳性率在IIa型达到峰值;MuSK抗体阳性患者相对罕见,主要集中于b亚型组,且该组患者心脑血管疾病发生率高于a亚型组[1]。
BEYOND研究:gMG患者的残留症状及日常生活负担
BEYOND研究聚焦gMG患者经治后的残留症状及其变化情况,并分析了这种症状波动对患者日常生活造成的影响。研究纳入14例女性患者和5例男性患者,目前主要接受糖皮质激素(n=12)、胆碱酯酶抑制剂(n=12)、免疫抑制剂(n=9)、血浆置换/IVIg(n=4)治疗,少数患者接受C5补体抑制剂(n=1)、FcRn拮抗剂(n=1)和抗CD20单抗(n=2)治疗,患者接受治疗后均有残留症状。结果显示,各有超过60%的患者报告残留症状显著影响其家务劳动、个人爱好、社会交往、职业/学业能力及未来发展规划,80%及以上患者赞同,若症状获得更好控制,将显著提升其生活质量满意度,具体表现为可更自主地参与偏好活动。该研究突破了临床医生认知,从患者视角全面呈现gMG残留症状负担,为改善患者生活提供依据[2]。
真实世界研究:中国gMG急性加重患者的治疗模式与经济负担
该项真实世界研究聚焦中国gMG急性加重患者治疗模式与经济负担,将收集包括人口统计学信息、病史、体格检查、MG相关量表评分、实验室检查等临床数据,数据收集目前已收集15个研究中心的476例患者数据,剩余数据持续收集中。分析包括住院时长、费用、置管时间、ICU停留时长等疾病负担以及挽救性治疗(如 IVIG/PE 等)、急性期治疗相关费用等治疗负担,还将分析感染率、气管切开频率、并发症、全因死亡率等指标。目前研究已在数据收集和分析上取得阶段性成果,随着研究推进,有望为中国gMG急性加重患者的临床治疗及经济负担管理,提供重要科学依据与实践指导[3]。
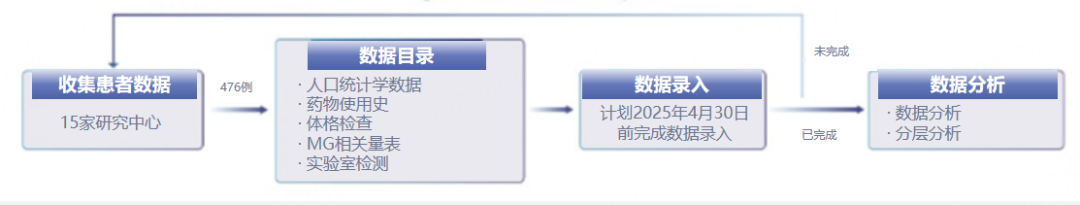
图1 研究设计
补体C5抑制剂治疗gMG的临床研究进展
MG是一种由自身抗体介导的神经肌肉接头疾病,其中补体激活在AChR抗体阳性MG的发病机制中起关键作用。近年来,补体C5抑制剂的出现为MG的治疗提供了新的靶向干预策略。本次EAN大会上多项关键研究探索了补体C5抑制剂在gMG中的治疗潜力。这些真实世界与前瞻性研究不仅验证了补体抑制剂的疗效和安全性,还为精准分层治疗提供了循证依据,推动MG从传统免疫抑制向靶向治疗的范式转变。
研究亮点导读:
单中心队列研究:依库珠单抗治疗难治性AChR抗体阳性gMG的快速起效策略:难治性AChR抗体阳性gMG患者经依库珠单抗治疗5周内MG-ADL评分下降73%,疗效持续稳定,不良事件轻微,显示依库珠单抗在真实世界中快速起效,为治疗难治性gMG提供了依据[4]。
德国真实世界研究:通过TSQM-9量表量化表明瑞利珠单抗在治疗便利性和提升总体满意度方面的优势,该研究从“以患者为中心”角度验证长效补体抑制剂对gMG患者[n=62,其中59例(95%)患者AChR抗体阳性]治疗依从性和生活质量的改善价值[5];
全球注册研究为降低免疫抑制剂负担提供治疗依据:该研究显示引入瑞利珠单抗治疗AChR抗体阳性gMG后30.3%患者成功减停1种及以上联合免疫抑制剂,76.9%患者泼尼松使用剂量降低至10mg/天及以下。该研究显示瑞利珠单抗的“免疫抑制剂减负治疗”潜力[6]。
补体C5抑制剂Zilucoplan治疗AChR抗体阳性gMG的真实世界研究:该项真实世界研究评估了Zilucoplan治疗AChR抗体阳性gMG患者的疗效和安全性,最终认为Zilucoplan为难治型MG患者提供了一种高效、安全性良好且易于使用的新疗法,但仍需更大样本和长期观察以进一步验证疗效与安全性[7]。
单中心研究:依库珠单抗在难治性AChR抗体阳性成人gMG患者中快速起效
该研究纳入8例AChR抗体阳性难治性成人gMG患者,给予依库珠单抗治疗,在治疗前(T0)、治疗5周后(T1)及之后每隔3个月(T2)进行数据评估。其中25%的患者有胸腺瘤手术史。结果显示,治疗5周后,患者MG-ADL平均评分从基线的8.38分降至治疗后降至2.13分(P = 0.001),QMG评分从基线13.75分降至5.63分(P = 0.001),后续随访中保持稳定改善。从T0至T1,MG-ADL评分的平均变化百分比为-73%(±20%),表明患者日常生活活动执行能力得到显著、快速改善。在安全性方面,所有患者在治疗前都接种了脑膜炎球菌疫苗,随访期间无患者出现疑似脑膜炎球菌感染症状,37%患者未报告任何不良事件,余63%患者报告了头痛(25%)、肺炎(25%)和COVID19(12.5%),无患者出现临床症状恶化或需求进行挽救治疗。该单中心研究显示,在真实医疗环境中依库珠单抗对于AChR抗体阳性难治性gMG患者的疗效显著且持久,这些发现与REGAIN研究中的结果一致[4]。
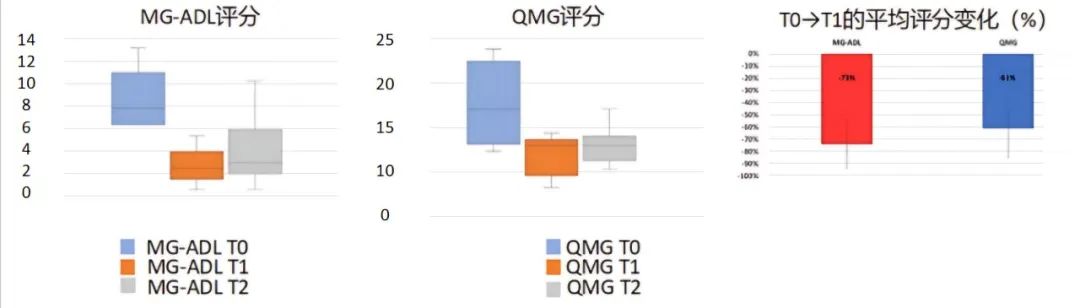
图 3 患者接受依库珠单抗治疗后MG-ADL和QMG评分变化
德国真实世界研究:瑞利珠单抗治疗gMG患者的真实疗效与安全性安徽润格
该项前瞻性多中心观察性研究纳入德国6家中心、62例gMG患者[含补体抑制剂初治者、从依库珠单抗转换为瑞利珠单抗者,其中59例(95%)患者AChR抗体阳性,患者基线时合并泼尼松、硫唑嘌呤、吗替麦考酚酯、甲氨蝶呤治疗],旨在评估患者接受瑞利珠单抗治疗期间的满意度。结果显示,在瑞利珠单抗治疗6个月期间,通过治疗满意度问卷(TSQM-9)评估,“便利性”“有效性”“总体满意度” 等子维度随治疗呈现积极变化,患者对瑞利珠单抗治疗的整体满意度提升。在疗效方面,患者MG-ADL、QMG等评分改善,治疗26周内症状逐步缓解,临床效果与既有认知一致;在安全性方面,仅发生2例严重不良事件(胰腺炎、蜂窝织炎 ),均判定与瑞利珠单抗无明确关联;未出现脑膜炎球菌感染,安全性良好。该研究认为瑞利珠单抗治疗gMG在真实世界中展现出良好的安全性、有效性,能提升患者满意度[5]。
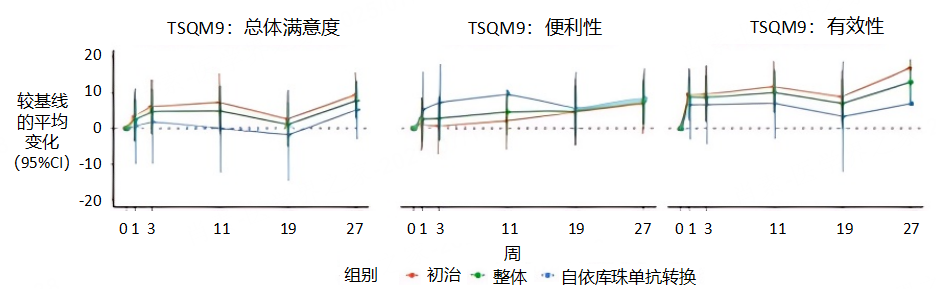
图 9 瑞利珠单抗治疗期间患者满意度变化
聚焦激素减量,瑞利珠单抗助力gMG个体化治疗策略
该项全球 MG SPOTLIGHT注册研究(NCT04202341)旨在评估瑞利珠单抗在AChR抗体阳性gMG 患者中的临床结局,通过分析瑞利珠单抗治疗后患者联合免疫抑制剂的使用变化,探讨其减少激素依赖的潜力。纳入接受瑞利珠单抗治疗≥6个月且具有完整联合免疫抑制剂(ISTs)治疗(包括硫唑嘌呤、吗替麦考酚酯、静脉注射免疫球蛋白/血浆置换、甲氨蝶呤及OCS)数据的患者。共纳入44例患者符合分析标准(男性70.5%;入组平均年龄68.3±13.0岁;瑞利珠单抗平均治疗时长1.3±0.8年)。经瑞利珠单抗治疗后,33例患者中有10例(30.3%)停用≥1种联合ISTs,其中3例(30%)和8例(80%)分别于治疗开始后3个月内和6个月内实现停药。每日OCS用量≤5mg和≤10mg的患者比例从基线时的11/26例(42.3%)和16/26例(61.5%),分别提升至治疗3个月后的14/26例(53.8%)和20/26例(76.9%),以及治疗6个月后的16/26例(61.5%)和20/26例(76.9%) [6] 。
在安全性方面,瑞利珠单抗耐受性良好,与既往分析和临床试验数据一致。研究观察到,瑞利珠单抗治疗可减少AChR抗体阳性gMG 患者对联合免疫抑制剂和OCS的依赖,表现出降低激素剂量的作用[6]。
补体C5抑制剂Zilucoplan治疗AChR抗体阳性全身型重症肌无力的真实世界研究
本研究基于同情用药项目GM0025IT,评估了Zilucoplan治疗AChR抗体阳性gMG患者的疗效和安全性。共纳入15例病情严重、治疗需求高的患者(女/男12/3,平均年龄55岁),每日自行皮下注射Zilucoplan,原有药物维持不变。疗效主要通过MG-ADL和QMG评分动态监测。结果显示,Zilucoplan首次注射一周后即观察到MG-ADL评分较基线(10.4±3.5分)下降,平均改善1.67分(范围-4至0分)。第4周和第24周时分别改善3.8分和7.27分。QMG评分方面,第4周和第24周较基线(16.5±5.7分)分别下降3.86分和7.28分。患者对药物耐受良好、自主注射便利,安全性突出。该研究认为Zilucoplan为难治型MG患者提供了一种高效、安全性良好且易于使用的新疗法,但仍需更大样本和长期观察以进一步验证疗效与安全性[7]。
临床突破与多元进展:NMOSD 诊疗新路径探索
NMOSD作为一种自身免疫性神经系统疾病,妊娠患者的治疗、个体化治疗及与风湿性疾病共病的复杂诊疗均为临床难题。以下通过本次EAN大会上的3项研究,包括依库珠单抗在孕期 NMOSD 复发中的应用、其疗效与基因多态性的关联,以及抗IL-23疗法用于NMOSD合并风湿性疾病的尝试,为突破诊疗困境提供新方向,同时剖析NMOSD诊疗在特殊人群、精准医学及共病管理维度的探索与进展。
研究亮点导读
依库珠单抗治疗1例妊娠期间复发的AQP4抗体阳性NMOSD:该病例报道首次显示依库珠单抗在妊娠中晚期(16-38周)应用的安全性,支持依库珠单抗作为孕期AQP4抗体阳性 NMOSD 的预防复发治疗的安全性,虽需更大样本确证新生儿安全性及优化剂量,但良好结局体现了该药物的安全性[8];
基因导向的生物制剂精准治疗突破:该研究首次发现rs17611 C>T变异携带者对依库珠单抗反应更佳(EDSS改善幅度提高50%),揭示亚洲人群特有的治疗优势。该研究提出首个基于基因多态性的NMOSD分层治疗策略,推动补体抑制剂从“经验用药”到“基因检测指导用药”的范式转变[9]。
抗IL-23疗法治疗NMOSD合并多种风湿性疾病的病例报告:该病例报告了一名例58岁合并多种风湿性疾病的NMOSD 女性患者的疾病历程,患者病情出现进展与恶化后原有免疫抑制治疗方案疗效不佳,换用IL-23抑制剂后实现病情控制[10]。
依库珠单抗治疗1例妊娠期间复发的AQP4抗体阳性NMOSD
1名27 岁女性孕16周时AQP4抗体阳性NMOSD复发,EDSS评分为7.0。孕16周起用依库珠单抗治疗,首月900mg /周,次月1200mg两周一次;孕38周剖宫产,胎儿无异常,新生儿为2.7kg男婴,1、5、10分钟Apgar评分均为10分;孕期除,无子痫前期、子痫等并发症,NMOSD未再复发。 该病例支持依库珠单抗作为孕期AQP4抗体阳性 NMOSD 的预防复发治疗的安全性,虽需更大样本确证新生儿安全性、优化剂量,但良好结局体现其安全性,有生育需求的NMOSD患者,孕前咨询和多学科照护仍很关键[8]。
依库珠单抗治疗亚洲AQP4抗体阳性 NMOSD患者的疗效与基因多态性有关
该项前瞻性观察性研究旨在评估依库珠单抗在中国AQP4抗体阳性 NMOSD 患者中的临床疗效,及其与 rs17611 基因多态性的相互作用,以优化个性化治疗方案。共纳入2024 年 8 月至2025年3月期间,中南大学湘雅医院5例急性发作的 AQP4-IgG 血清阳性 NMOSD 患者。该研究发现,rs17611 C>T 变异携带者(n=2):EDSS 评分改善更显著,中位降低 1.5 分(范围 1.0-2.0),优于野生型患者(n=3)的中位降低 1.0 分(范围 1.0-1.5,P=0.042)。结果提示,rs17611可能是潜在的NMOSD 精准给药的生物标志物,建议在亚洲人群中采用基因型指导的剂量递增方案[9]。
抗IL-23疗法治疗NMOSD合并多种风湿性疾病的病例报告
NMOSD常与其他自身免疫性疾病共存,IL-23 抑制剂此前用于治疗风湿性疾病,但在 NMOSD 单药治疗或联合治疗中其疗效和安全性数据有限。该研究报道了58 岁女性患者,患有多种风湿性疾病(播散性脓疱性银屑病、干燥综合征、结节性痒疹 )和 NMOSD ,2012年时患者出现单侧视神经炎,予以糖皮质激素和甲氨蝶呤(MTX)治疗,2014年患者复发,出现多发幕上和幕下强化病灶、脑脊液细胞增多,血清AQP4抗体阳性,加用利妥昔单抗(RTX),2014~2022患者病情稳定,维持低剂量激素和MTX和规律RTX治疗。2023~2024年患者出现风湿性和皮肤疾病恶化,对高剂量糖皮质激素和MTX无反应,采用抗IL-23(Guselkumab)联合RTX治疗后实现良好的整体控制。该研究认为除抗CD20等常用于NMOSD 的药物外,IL-23抑制剂或可成为这类患者管理的新治疗选择,且目前未记录到重大安全警告 [10] 。
结语
从本次EAN2025年会公布的研究成果来看,生物制剂在神经免疫疾病领域的突破正重塑MG与NMOSD的治疗格局。在MG领域,无论是依库珠单抗对难治性AChR抗体阳性成人gMG患者的快速起效、瑞利珠单抗在激素减量中的优势,还是MG自身抗体聚类分析,研究证实补体靶向治疗已从“对症干预” 迈向 “精准调控”;而在NMOSD治疗领域,上述研究则为罕见病妊娠管理与精准医疗提供了新范式探索。
参考文献:
[1] M. Qu, X. Rong, M. Liu, et al. Autoantibodies in myasthenia gravis: Cluster analysis, and clinical correlations.EAN 2025, EPO-305.
[2] Francesco Saccà, Sophie Lehnerer, Maria (Maya) Bonaria Uccheddu, et al. Burden of remaining symptoms and fluctuations of generalized myasthenia gravis on patients' daily lives – BEYOND study. EAN 2025, EPO-108.
[3] T. Xu, W. Yin, H. Yang et al. A Real-world Study on the Treatment and Economic Burden of Generalized Myasthenia Gravis Acute Exacerbation in China. EAN 2025, EPV-657.
[4] F. D'Anna, G. D'Alvano, V. Todisco, et al. Rapid onset of efficacy of Eculizumab in single-center cohort of patients with refractory generalized Myasthenia Gravis. EAN 2025, EPO-295.
[5] Lea Gerischer, Maike Stein, Frauke Stascheit, et al. Evaluating Ravulizumab in generalized Myasthenia Gravis: Patient Satisfaction and Real-World Evidence from Germany.EAN 2025, EPV-665.
[6] R. Nowak, A. Habib, A. Meisel, et al. Concomitant immunosuppressive therapy use with Ravulizumab: Analysis of a generalized myasthenia gravis global registry.EAN 2025, EPR-297.
[7] N. Rini, P. Luppino, P. Alonge, et al. A real-life experience with zilucoplan in AChR-seropositive generalized myasthenia gravis.EAN 2025, EPR-308.
[8] Benjian Sun, Lijia Zou, Fen Li, et al. A First Chinese Case Rport: Successful Management of Relapsed AQP4-lgG Neuromyelitis Optica Spectrum Disorder During Pregnancy with Eculizumab.EAN 2025, EPV-841.
[9] L. Zou, J. Li, S. Chen, et al. Efficacy of Eculizumab and Pharmacogenetic Modulation by rs17611 in Chinese AQP4-IgG-Positive Relapsing Neuromyelitis Optica Spectrum Disorder: Implications for Precision Dosing.EAN 2025, EPO-637.
[10] M. Morra, E. Virgilio, F. Masuzzo, et al.Treatment of NMOSD and multiple rheumatologic comorbidities with anti-IL23 Therapies: a case report. EAN 2025, EPV-842.
疫苗声明:
所有使用依库珠单抗的患者必须接种四价脑膜炎疫苗(ACYW135),在有条件的情况下接种B型疫苗,详细请见依库珠单抗注射液说明书【注意事项】。
本材料由阿斯利康提供,仅供医疗卫生专业人士进行医学科学交流,不用于推广目的。审批编码:CN-162445 过期日期:2025-10-10
*此文仅用于向医学人士提供科学信息,不代表本平台观点

华泰优配提示:文章来自网络,不代表本站观点。